Uma ciência de verdade se faz com o debate aberto de ideias e com a cuidadosa reanálise e/ou replicação dos resultados por outros pesquisadores para que sejam confirmados ou refutados. Para que isso ocorra, é necessário que os bons princípios da ciência sejam seguidos em todas as etapas, incluindo a independência dos pesquisadores, a objetividade dos estudos e a transparência dos dados. Afinal, se o objetivo verdadeiro das pesquisas científicas for de fato melhorar a saúde das pessoas – em vez de simplesmente engordar a fortuna da indústria – quanto mais aberta e neutra for a ciência, melhor para todos.
Um dos maiores problemas na atualidade é que 75% das pesquisas clínicas em medicina são patrocinadas e conduzidas pela própria indústria farmacêutica que produz e vende a preços aviltantes os seus produtos[1]. Isso significa que existe muito dinheiro em jogo ao se realizar os estudos científicos. Um ensaio clínico que demonstre algum benefício com o uso de determinada droga costuma representar muitos bilhões de dólares a mais no caixa da empresa. Isso é mais que suficiente para distorcer delineamentos, turvar limites éticos e suprimir resultados desagradáveis. Além disso, quando os pesquisadores recebem quantias vultosas diretamente da indústria que produz os medicamentos testados temos um senhor conflito de interesses difícil de mensurar e ainda mais difícil de aceitar.
Um bom exemplo é a história da droga evolocumabe, um anticorpo monoclonal recentemente lançado para controle do colesterol LDL e que também poderia trazer benefícios clínicos relevantes. Essa história nos ajuda a entender como realmente funciona na prática essa coisa que nos acostumamos a chamar de ciência, mas que de ciência verdadeira talvez tenha muito pouco. Talvez essa narrativa também nos ajude a perceber melhor o problema do crescente descrédito da ciência e possa nos levar a mudar a nossa forma de financiar e conduzir estudos clínicos.
A publicação do estudo é comemorada (com sorrisos amarelos)
Em meados de 2017 foi publicado no New England Journal of Medicine o famoso estudo FOURIER, um ensaio clínico randomizado no qual foi testada uma nova droga injetável (evolocumabe), a qual reduziria os níveis de colesterol LDL em pessoas que já usavam estatinas, mas que ainda apresentavam LDL acima de 70 mg/dL. A ideia era de que o LDL deveria ser “quanto mais baixo melhor”, e que isso poderia trazer benefícios clínicos para as pessoas. De fato, o estudo mostrou uma redução grande (59%) nos níveis de LDL e resultou em uma redução absoluta bem mais modesta (1,5%) no risco de um desfecho clínico composto por morte cardiovascular, infarto e AVC. A diferença foi estatisticamente significativa e resultaria em um NNT de 67 (isso significa que 67 pessoas teriam que ser tratadas durante cerca de 2 anos para que evitasse o desfecho em uma única pessoa).
Porém, alguns detalhes precisam ser salientados. Em primeiro lugar, o estudo foi patrocinado pela própria Amgen, empresa fabricante da droga e que delineou o estudo, coletou os dados e, principalmente, financiou o trabalho dos pesquisadores, os quais foram muito bem pagos pela indústria (vários eram até mesmo funcionários efetivos da empresa). Além disso, trata-se de um estudo de prevenção secundária em pacientes de risco muito alto que eram em sua maioria homens (75%) idosos (média de 63 anos), com alta prevalência de diabetes, hipertensão e tabagismo, que tinham sofrido infarto ou AVC recentemente e já faziam uso de estatinas para controle do colesterol (em sua maioria com doses elevadas). Isso tudo sugere que o benefício clínico real seja bem menor se a droga for usada em populações mais abrangentes e com doença menos grave.
Os critérios de exclusão também eram amplos, excluindo pessoas com insuficiência renal, histórico de AVC hemorrágico, insuficiência cardíaca e hipertensão não controlada, entre outras coisas. Também é importante notar que, embora o estudo tenha demonstrado redução no citado desfecho composto, não houve redução estatisticamente significativa quando se analisou individualmente desfechos importantes como mortalidade cardiovascular ou mortalidade total. Enfim, embora os dados tenham sido bastante comemorados por alguns, as ações da Amgen caíram logo após a publicação do estudo, o que sugere que os investidores não tenham levado muita fé na nova droga[2].

Os achados do estudo são refutados
Alguns anos mais tarde, um grupo de pesquisadores da Espanha e do Canadá reanalisou os dados do estudo para confirmar seus achados e publicou os resultados em 2021 no BMJ Open[3]. O estudo foi realizado como parte da iniciativa RIAT[4], uma empreitada internacional que visa restituir a visibilidade de estudos cujos dados permanecem inacessíveis a outros pesquisadores. Um detalhe importante é que, para terem acesso aos dados coletados dos pacientes durante o estudo, os pesquisadores tiveram que recorrer à agência reguladora de medicamentos do Canadá, uma vez que nem as outras agências nem os autores do estudo original consentiram em compartilhar seus dados.
Os achados dessa reavaliação mostraram inconsistências na atribuição dos desfechos clínicos em mais de 40% dos pacientes do estudo. O problema levantado pelos autores da reanálise foi de que, ao se reatribuir os desfechos conforme os dados clínicos obtidos, haveria um aumento do número de desfechos negativos no grupo de pacientes tratados com evolocumabe e uma redução de desfechos ruins no grupo de pacientes que receberam placebo. A diferença final não foi significativa a ponto de mostrar dano causado pela droga, mas tampouco mostrava qualquer benefício clínico relevante. Isso levou os pesquisadores que reanalisaram o estudo a sugerir, de maneira cautelosa, que houvesse um maior ceticismo em relação ao uso da droga naquele momento e que os dados originais do estudo inicial fossem tornados públicos – algo tão simples! – para que outros pesquisadores também pudessem reanalisá-los.
A ciência encolhe mais um pouco
Em uma troca de cartas[5] (e farpas) que se seguiu à publicação da reanálise do estudo, os pesquisadores originais defenderam seus dados sugerindo que as conclusões do grupo da reanálise estavam equivocadas porque eles não tinham tido acesso aos dados completos do estudo, o que gerou conclusões que consideravam ser sensacionalistas. Por sua vez, o grupo da reanálise respondeu que o acesso aos dados completos havia sido solicitado por eles próprios aos autores do estudo original e que a solicitação não tinha sequer sido respondida.
Enfim, houve uma troca de acusações que envergonha a própria ciência, uma vez que dados anonimizados de ensaios clínicos que envolvam seres humanos deveriam sempre ser disponibilizados a todos que os queiram analisar, para o bem dos pacientes e da própria ciência. Assim, de um lado podemos ter uma reanálise que foi incompleta porque dados importantes podem ter sido ativamente ocultados dos pesquisadores. De outro lado, temos pesquisadores que tratam dados científicos dos voluntários de estudos como se fossem dados comerciais sigilosos. Nada disso ajuda na recuperação da credibilidade da ciência, a qual infelizmente parece estar em queda livre.
Se escondo algo, o que escondo e por que o faço?
A questão que se impõe é: se os resultados dos estudos são realmente tão bons como defendem os pesquisadores do estudo original, então por que eles não podem ser tornados públicos? Afinal, isso reforçaria a importância de seus achados e aumentaria a credibilidade das pesquisas clínicas. Toda a empreitada científica corre risco se dados importantes são ocultados e não podem ser reanalisados por outros pesquisadores. Só quem ganha com esse mistério é a própria indústria farmacêutica e a mais recente e famigerada indústria das teorias conspiratórias. O que parece difícil de aceitar é que pesquisadores sérios, os quais deveriam ter a saúde da população e a ciência como objetivos principais, participem de um jogo de ocultação de dados que, no final das contas, prejudica aos pacientes e à própria ciência da qual fazem parte.
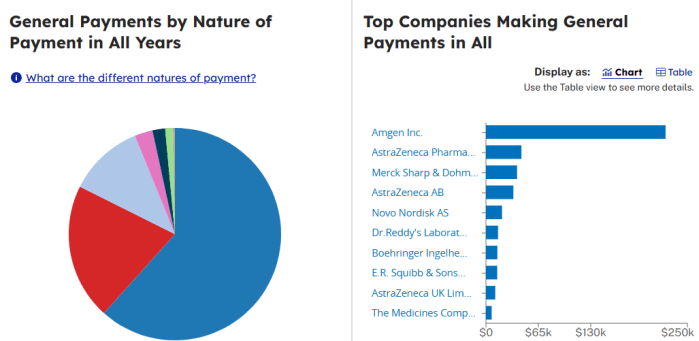
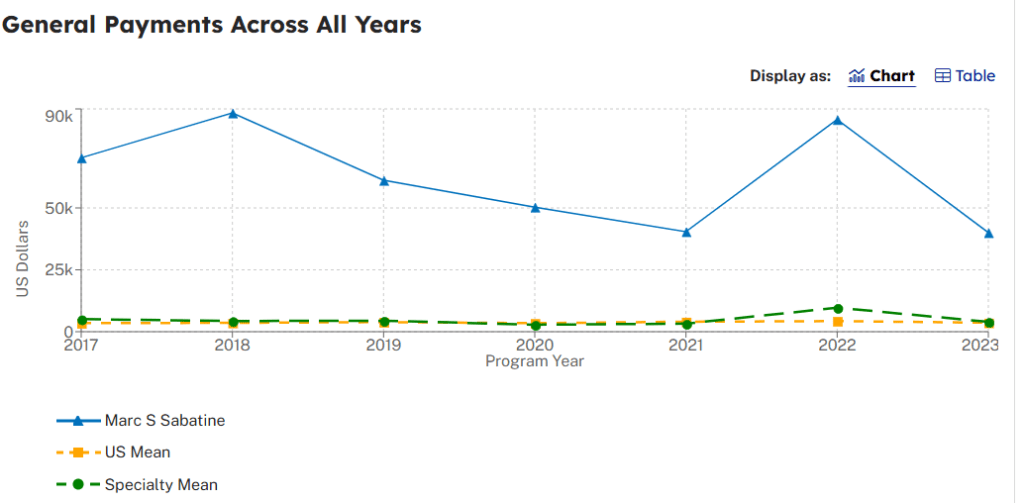
Se a opção por ocultar dados e tratá-los como sigilo comercial fosse apenas uma parte misteriosa da função do pesquisador, a coisa não seria tão triste. Mas nesse ponto é inevitável recorrer à questão dos conflitos de interesse financeiros para tentar compreender melhor a situação. Uma breve vasculhada na página da Open Payments[6] mostra que o principal pesquisador do estudo original tem recebido da indústria farmacêutica uma quantia que varia entre 50 e 100 mil dólares todos os anos entre 2017 (ano da publicação do estudo) e 2023. Além disso, não deve ser surpresa para ninguém que sua maior fonte pagadora é a própria Amgen, fabricante do evolocumabe. Como se isso não bastasse, o autor ainda recebeu nesse período vários milhões de dólares da mesma empresa sob a rubrica de “financiamento de pesquisas”. No total e apenas considerando as cifras declaradas ao sistema, o autor recebeu da Amgen no período citado mais de 200 mil dólares a título de “pagamentos gerais” (o que inclui palestras, consultorias e outras maneiras de compensação por serviços prestados) e mais de 12 milhões de dólares como “verbas para pesquisas”. Convenhamos que são valores suficientes para moldar pontos de vista e distorcer percepções.
Algumas reflexões constrangedoras
Esta não é uma crítica nem uma sugestão de ineficácia de uma determinada droga. Afinal, quem não gostaria que se descobrisse uma droga qualquer que pudesse reduzir o sofrimento causado pelas doenças cardiovasculares? Principalmente se a eficácia de tal droga fosse comprovada em estudos de qualidade, isentos de conflitos financeiros e que pudessem ser devidamente confirmados por outros pesquisadores. Também não se trata de crítica a um pesquisador em especial, pois o comportamento aqui citado é a regra atual nisso que resolvemos chamar de “ciência”. Se fizermos a mesma pesquisa no Open Payments com os autores principais de outros estudos importantes de drogas badaladas pela mídia obteremos resultados bastante parecidos.
Infelizmente, o problema é bem mais grave e parece estar muito mais entranhado na pesquisa clínica do que imaginamos, a ponto de muita gente dentro da medicina considerar absolutamente normal que pesquisadores embolsem fortunas da indústria farmacêutica para realizar estudos ou disseminar as narrativas que interessem a essa indústria. Que fique claro que não existe nada errado no fato de os pesquisadores serem adequadamente recompensados por um trabalho que algumas vezes é bastante árduo. O erro gritante está em aceitarmos que tal recompensa seja recebida diretamente da indústria farmacêutica, o que induz a vieses que muitas vezes são difíceis de perceber e quantificar, ainda mais quando os dados permanecem sigilosos. E as consequências desses vieses podem colocar em risco a saúde das pessoas e a própria sustentabilidade dos sistemas de saúde.

Se a droga supracitada se mostrar claramente eficaz em longo prazo isso será ótimo, mas apenas se isso for feito com honestidade e transparência, caso contrário servirá apenas para alimentar as teorias conspiratórias que envolvem a ciência atual. Não é possível que pesquisadores sérios defendam o modelo atual de sigilo dos dados e assinem contratos que os impedem de fazer declarações pessoais sobre os dados dos estudos. É fundamental percebermos que entre o sigilo comercial da indústria de um lado e a teoria conspiratória do outro existe um espaço imenso que pode ser usado para recuperar a credibilidade da ciência, mas isso passa necessariamente por uma mudança em nossa maneira de financiar as pesquisas clínica e na forma como publicamos – ou não – os dados completos dos estudos. Continuar com o modus operandi da ciência médica atual apenas aumentará essa nefasta polarização e nos levará a um tipo de “cientificismo obscurantista”, onde quanto mais estudos são realizados, menos se acredita neles.
[1] https://jamanetwork.com/journals/jama/fullarticle/196846
[2] https://www.cnbc.com/2017/03/17/amgens-cholesterol-fighting-drug-disappoints-shares-drop.html
[3] https://bmjopen.bmj.com/content/12/12/e060172
[4] https://restoringtrials.org/
[5] https://bmjopen.bmj.com/content/12/12/e060172.responses#response-to-dr-sabatine-et-al